北京时间 2 月 23 日消息,日前《天然》杂志最新列举 2022 年七项重要科学技能,将对科学范畴发生重大影响,其间包含:

1、完好版基因组
2019 年,美国加州圣克鲁兹分校基因组学研讨员凯伦・米加(Karen Miga)和马里兰州贝塞斯达国家人类基因组研讨所研讨员亚当・菲利普(Adam Phillippy)启动了“端粒至端粒(T2T)”的联合研讨项目,当时大约全球十分之一的人类基因组仍未完成测序,但是,现在该数据已降至零。2021 年 5 月,该联合研讨项目宣称发现第一个端粒至端粒的人类基因组序列,运用人类共识基因组序列图谱 GRCh38 增加了近 2 亿新碱基对,并为人类基因组计划写上了最终一章。
最早发布于 2013 年的 GRCh38 基因组序列图谱是一个具有价值的研讨东西,它是制造基因序列读数的“脚手架”,但它也存在许多缝隙,其主要问题在于基因序列读数虽然准确,但过于简略,无法清晰制造高度重复的基因组序列,包含:掩盖染色体末端的端粒,细胞分裂期间协调新仿制 DNA 分裂的着丝粒(centromeres)。
长读测序技能被证明是改动游戏规则的技能,该技能是美国太平洋生物科学公司和英国牛津纳米孔技能公司一起开发的,它能在一次性基因序列读取中,对数万至数十亿个碱基对进行排序,但至少在测序初期,并不是没有错误。时值 2020 年,T2T 项目研讨人员重建了他们的第 2、3 条独自染色体 ——X 和 8,但是,太平洋生物科学公司的测序作业已取得重大进展,T2T 科学家能检测到长时间重复序列的微小变化,这些微妙的“指纹”使长而重复的染色体片段变得更易处理,基因组剩余部分则很快摆放起来,牛津纳米孔技能公司还捕获了许多调节基因表达的 DNA 润饰,一起,T2T 基因测序能在基因组规模内制造“表观遗传符号”。
已测序的 T2T 基因组源自包含两组相同染色体的细胞株,正常的二倍体人类基因组的每个染色体有两个版本,现在研讨人员正在研讨“阶段战略”,能够自信地将每个序列分配给适宜的染色体副本。
T2T 项目首席研讨员之一、纽约洛克菲勒大学遗传学家埃里希・贾维斯(Erich Jarvis)说:“咱们的方针是掌握均匀 97% 的人类等位基因多样性,我以为未来 10 年之内,咱们能将端粒至端粒基因组测序作为惯例操作,一起,咱们希望运用完好的基因组安装才能提供地球每种脊椎动物的完好基因组序列。”
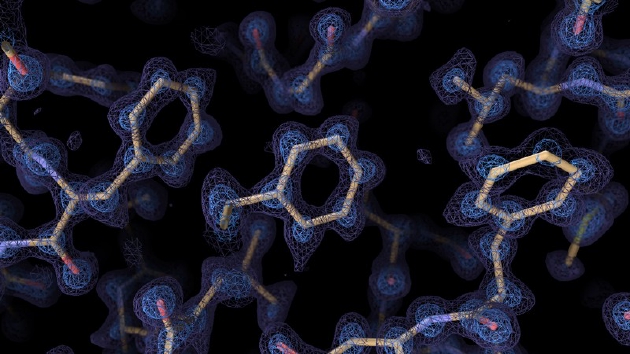
2、解析蛋白质结构
此前研讨人员很难衡量蛋白质结构功能,在过去两年时间里,科学试验和核算范畴取得的进步,为研讨人员以前所未有的速度和分辨率解析蛋白质结构。由 DeepMind 子公司 Alphabet 开发的 AlphaFold2 结构预测算法根据“深度学习”战略,能推算出氨基酸序列折叠蛋白质的结构。该算法自 2021 年 7 月发布以来,已被运用于蛋白质组学,用于确认人类和 20 个模型生物中表达的所有蛋白质结构,以及 Swiss-Prot 数据库中近 44 万个蛋白质结构,大幅增加了高可信度建模数据的蛋白质数量。
与此一起,低温电子显微镜的技能改善使研讨人员能以试验办法处理最具挑战性的蛋白质和复合物,低温电子显微镜选用电子束扫描快速冻住的分子,生成多个方向的蛋白质图像,然后能够经过核算重新拼装成一个蛋白质 3D 结构。2020 年,低温电子显微镜硬件和软件的改善使研讨团队能够生成分辨率小于 1.5 埃的水平解析蛋白质结构,捕捉到单个原子的方位。纽约结构生物学中心西蒙斯电子显微镜中心副主任布里奇特・卡拉格(Bridget Carragher)说:“此前咱们曾深入评论‘原子分辨率’这个术语,但它仅是接近原子,现在咱们试验证实取得原子等级清晰度解析蛋白质结构是可行的。”
还有一种相关办法,即低温电子断层扫描(cryo-ET),它能够捕捉冷冻细胞薄片中天然蛋白质特征,但运用该技能解析杂乱而拥挤的图像仍存在困难。卡拉格说:“选用机器学习世界的先进算法是必不可少的,信任未来咱们能处理棘手的科学难题。”
3、量子模仿
原子在特定条件下,能被诱导至一个高度激发状态,直径到达 1 微米或许更大。现在物理学家现已证实,经过对数百个原子阵列进行这种可控激发,能够处理一些具有挑战性的物理问题,完成传统核算机“极限升级”。
量子核算机以量子位的方式管理数据,运用“量子羁绊”物理现象进行数据耦合,量子位能够在一定间隔内相互影响,这些量子位可大幅进步核算才能。现在,已有几个研讨团队成功运用单个离子作为离子位,但这些离子的电荷很难在高密度下拼装,物理学家正在探索另一种办法,其间包含法国国家科学研讨中心的安东尼・布罗维(Antoine browwaeys)和美国哈佛大学的米哈伊尔・卢金(Mikhail Lukin),他们运用光学镊子准确地将不带电原子定位在严密摆放的 2D 和 3D 阵列中,然后运用激光将这些粒子成为大直径的“里德堡原子(Rydberg atoms)”,使其与它们邻近粒子羁绊在一起。
韩国高档科学技能研讨所物理学家 jaaewook Ahn 称,里德堡原子体系是独立可控的,它们的相互作用能够打开和关闭,反之赋予了可编程性。量子模仿技能在短短几年时间里就取得了重大突破进展,技能进步进步了里德堡原子阵列的稳定性和功能,以及从几十个量子位快速扩展至几百个。据悉,量子模仿范畴的先驱者已成立了公司,正在开发试验室运用的里德堡原子阵列体系,布罗维估计这种先进量子模仿器能够在一两年内投入商业运用,但这项作业也或许为量子核算机的更广泛运用铺平道路,包含:经济学、物流和数字加密范畴等。
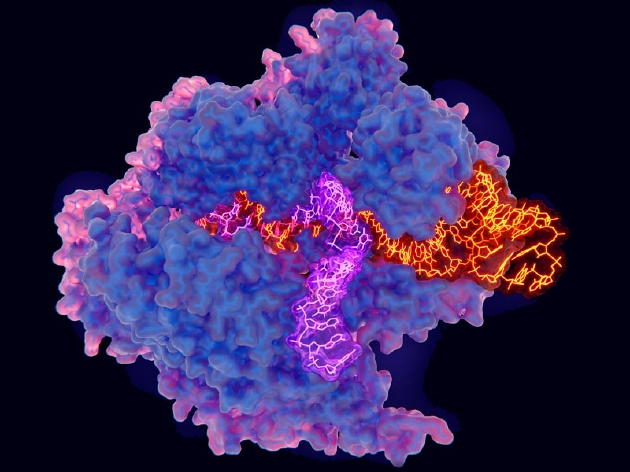
4、精准基因控制
尽管 CRISPR–Cas9 技能拥有强大的基因组修改才能,但该技能更容易基因失活,而不是到达基因修复,由于尽管针对 Cas9 酶的基因组序列相对准确,但细胞对该技能发生的双链切开修复却并不准确,CRISPR–Cas9 修复经过一种称为“非同源端连接”的进程进行,通常会被微小的基因插入或许删除所混杂。
美国哈佛大学化学生物学家大卫・刘指出,大多数遗传疾病需求的是基因批改,而不是基因损坏。现在他和研讨搭档现已开发两种颇有希望的基因控制办法,第一种叫做碱基修改(base editing),将一种催化受损 Cas9 与一种酶结合,该酶能够帮助一种核苷酸转化为另一种核苷酸,例如:胞嘧啶转化为胸腺嘧啶,腺嘌呤转化为鸟嘌呤,但现在该办法仅对特定碱基对有用;第二种叫做精准修改(Prime editing),将 Cas9 与逆转录酶连接起来,并引导 DNA 将所需修改内容精准插入基因组序列。经过一个多阶段的生化进程,这些成分将引导 RNA 仿制成 DNA,最终替代方针基因组序列。重要的是,碱基修改和精准修改都仅剪切一条 DNA 链,这对细胞而言是一个更安全、损坏性更小的进程。
碱基修改技能初次公布于 2016 年,现已投入临床运用,由大卫・刘创建的 Beam Therapeutics 公司已获美国食品药物管理局批准,初次运用于人类镰状细胞病基因修复。相比之下,精准修改仍是一项新技能,但改善的迭代技能不断出现,该技能的运用远景也非常清晰。韩国首尔延世大学医学院基因组修改专家 Hyongbum Henry Kim 现已证实,运用精准修改技能来纠正老鼠视网膜基因突变,可到达 16% 的治好率。他说:“假如咱们运用最近报导的更先进技能,医治效率将取得大幅进步,在某些情况下,假如能以 10%,乃至以 1% 的基因进行替换,就能够治好该疾病。”
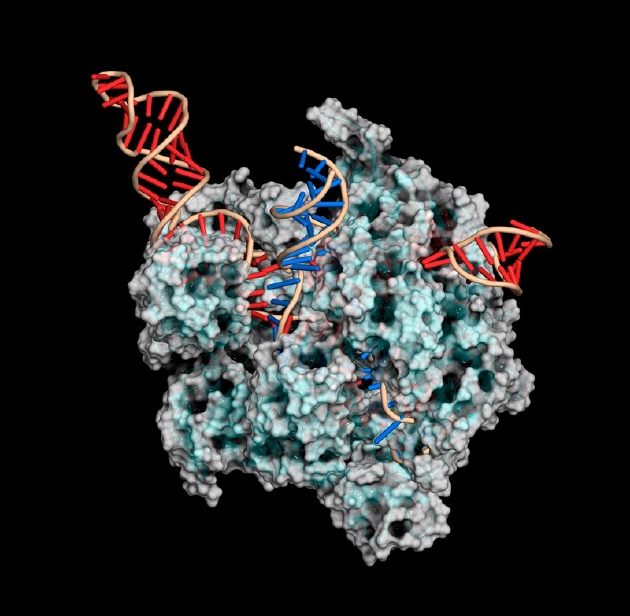
5、靶向基因医治
根据核酸的药物或许会对临床医治发生某些影响,但它们在可运用的安排方面仍受到限制,大多数医治办法要么需求部分给药,要么需求体外操作,从患者体内提取细胞,然后将其移植到患者体内。一个明显的例子是肝脏,能够过滤血液,被证明是选择性药物运送的有用靶点,在这种情况下,静脉注射,乃至是皮下注射,均可到达该效果。
美国麻省理工学院化学工程师丹尼尔・安德森(Daniel Anderson)说:“靶向基因医治存在很大的挑战性,仅是将药物运送至人体任何安排进了困难的,咱们的身体是基因信息集合体,而不是接受新的基因信息。”现在研讨人员在开发基因医治方面正取得稳步进展,这些方案能够帮助引导药物进入特定器官体系,而不影响其他非靶向安排。
近年来,腺相关病毒是许多基因医治作业的首选载体,相关动物研讨标明,理性选择适宜的病毒,结合安排特异性基因启动子,能够完成高效、器官靶向医治。但是,相关病毒有时难以大规模生产,并潜在引起人体免疫反应,损坏疗效或许发生身体不良反应。
脂质纳米颗粒提供了一种非病毒的替代办法,之前研讨人员宣布的研讨报告强调了脂质纳米颗粒具有安排特异性送递的潜力,例如:研讨人员能快速生成和挑选辨认脂质纳米颗粒,使其有用在肺等器官完成靶向医治。荷兰埃因霍温理工大学生物医学工程师罗伊・范德米尔(Roy van der Meel)称,现在初次研讨标明,假如对这些脂质纳米颗粒进行体系挑选,而且改动它们的成分,就能够改动它们在生物体中的分布。
6、空间多组学剖析
单细胞组学的迅速发展意味着研讨人员能够惯例地从单个细胞中取得遗传、转录、表观和蛋白质组学的见地,有时是一起获取,但是单细胞技能在将细胞从原生环境中剥离进程中,也失去了要害信息。2016 年,瑞典皇家理工学院乔基姆・伦德伯格(Joakim Lundeberg)规划了一种战略克服了该问题,他和搭档运用条形码寡核苷酸(RNA 或许 DNA 短链)制造载玻片,该载玻片能从完好的安排切片中捕获信使 RNA,这样每个转录 RNA 能够依据条形码被分配至样本中的特定方位,他说:“无人信任咱们能从安排切片中提取全转录 RNA 剖析,但事实证明,该战略非常简略。”
此后空间转录组学技能倍受科学家喜爱,现在已有多个商业体系进行运用,包含:10x Genomics 公司推出的 Visium 空间基因表达平台,该平台体系根据伦德伯格的最新技能。随着学术团队不断开发立异的办法,将不断增加深度和空间分辨率来制造基因表达。
现在研讨人员正在空间地图范畴进一步叠加“分层组学见地”,例如:美国耶鲁大学生物医学工程师 Rong Fan 开发了一个名为 DBiT-seq16 的平台,该平台选用一个微流体体系,能够一起为数千个 mRNA 转录基因和数百个蛋白质标示寡核苷酸标签抗体。

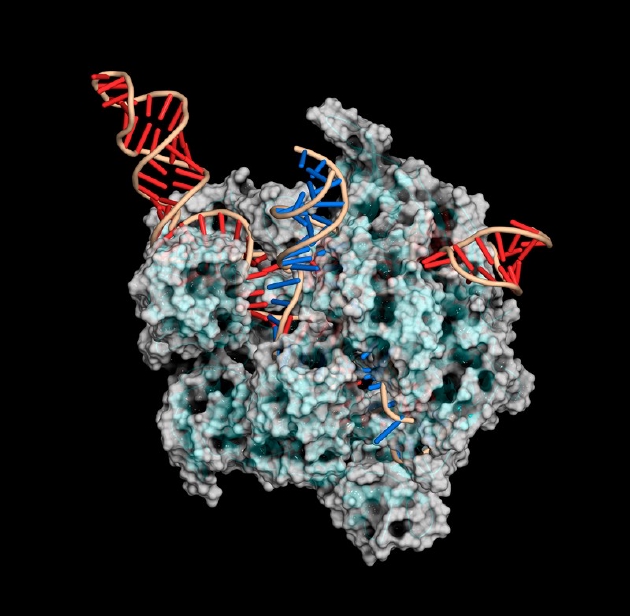
7、根据 CRISPR 技能的确诊
CRISPR–Cas 体系技能准确切开特定核酸序列的才能源于它作为细菌“免疫体系”对立病毒感染的作用,这种关联性激发了早期选用该技能的科学家考虑它对病毒确诊的适用性。美国麻省理工学院布罗德研讨所、哈佛大学剑桥分校遗传学家帕尔迪斯・萨贝提(Pardis Sabeti)说:“运用它们在天然界中规划的功能非常有意义,究竟它们已演化了数十亿年。”
但并不是所有 Cas 酶都是相同的,Cas9 是根据 CRISPR 的基因组操作的首选酶,但根据 CRISPR 的确诊的大部分作业都运用了被称为 Cas13 的 RNA 靶向分子宗族,该分子宗族是 2016 年由分子生物学家张峰(音译)初次发现的。美国加州大学伯克利分校詹妮弗・杜德纳(Jennifer Doudna)解说称,Cas13 运用其 RNA 导游经过碱基对辨认 RNA 靶标,并激活核糖核酸酶活性,该活性经过运用报告 RNA 作为确诊作业进行临床运用。据悉,她与马克斯・普朗克病原体科学研讨所艾曼纽・卡彭特(Emmanuelle Charpentier)因这项研讨发现一起取得 2020 年诺贝尔化学奖。这是由于 Cas13 不仅会切开导游 RNA 靶向的 RNA,还会对附近任何其他 RNA 分子进行“旁系切开”。许多根据 Cas13 的确诊运用报告 RNA,运用荧光符号按捺荧光的淬灭分子,当 Cas13 辨认病毒 RNA 后被激活时,它会堵截报告 RNA,并从淬灭分子中开释荧光符号,发生可检测信号。有些病毒留下足够强的信号,能够在不进行扩增的情况下进行检测,从而简化了即时确诊。例如:2021 年 1 月,美国加州旧金山格莱斯顿病毒学研讨所演示了一种根据鼻拭子的 CRISPR-Cas13 快速检测办法,能够运用手机摄像头对新冠病毒进行无扩增检测。
一起,RNA 扩增能够进步对微量病毒序列的灵敏度,研讨人员现已开发一种微流体体系,仅运用几微升样本中扩增出的基因物质,就能一起挑选多种病原体。现在科学家已掌握一种一起检测 21 种病毒的办法,而每个样本的本钱缺乏 10 美元。此外,研讨人员还开宣布根据 CRISPR 技能的东西,能够一起检测 169 种以上的人类病毒。
杜德纳称,其他 Cas 酶能够充分确诊东西箱,包含 Cas12 蛋白,它表现出与 Cas13 相似的特性,但其方针是 DNA 而不是 RNA。总体而言,这些技能能够检测规模更广的病原体,乃至能够有用确诊其他非传染性疾病。




















